Der neue RSV- Impfstoff von Pfizer für ältere Erwachsene kann das potenziell tödliche Guillain-Barre-Syndrom (GBS) auslösen, warnt die Lebensmittel- und Arzneimittelbehörde Food and Drug Administration (FDA).
In klinischen Studien entwickelten zwei Teilnehmer in ihren 60er-Lebensjahren den Zustand, der auch lähmende Schmerzen, Muskelschwäche und Lähmungen verursachen kann. Einer der Patienten erholte sich nach drei Monaten, aber der zweite brauchte sechs Monate, um wieder ohne Beschwerden zu sein. Sie gehörten zu den 20.000 Erwachsenen, die die experimentelle Spritze bekamen.
In der Kontrollgruppe, die den Impfstoff nicht erhielt, gab es keine Fälle von GBS, was die FDA dazu veranlasst hat, Pfizer zu bitten, vor der Zulassung des Impfstoffs eine Sicherheitsüberprüfung durchzuführen.
Mehrere Pharmaunternehmen entwickeln einen Impfstoff gegen das Respiratory Syncytial Virus (RSV), eine winterliche Atemwegsinfektion, die in den USA jedes Jahr bis zu 10.000 Erwachsene über 65 tötet. Derzeit ist kein Impfstoff gegen die Krankheit verfügbar.

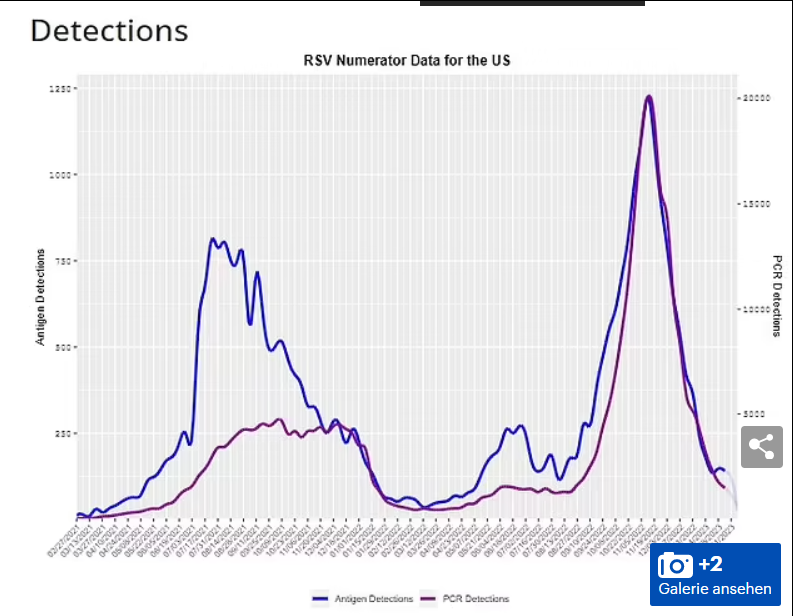
Die Krankheit ist weit verbreitet, wobei die Fälle in diesem Jahr ohne Covid-Beschränkungen zunehmen (Bild).
Ältere Erwachsene sind durch die Krankheit stärker gefährdet, da sie ein schwächeres Immunsystem haben.
Guillain-Barre sieht, wie das Immunsystem verrückt spielt und anfängt, Nervenzellen anzugreifen, was Symptome wie Muskelschmerzen, Taubheitsgefühl und Kribbeln auslöst. Es wurde auch bei Versuchen mit einem konkurrierenden RSV-Impfstoff des britischen Pharmariesen GSK aufgezeichnet. Der Zustand wurde zuvor auch bei Personen gemeldet, die den Covid-Impfstoff von AstraZeneca erhielten, der in den USA nicht zur Verwendung zugelassen war.
Einer der Patienten, die das Syndrom in Pfizers Studie entwickelten, war ein Amerikaner in den Sechzigern mit einer Vorgeschichte von Bluthochdruck. Er litt acht Tage nach der Impfung unter Rückenschmerzen und am 14. Tag an Schwäche in seinen Beinen. Nach einem Sturz wurde der Mann ins Krankenhaus eingeliefert und anschließend mit dem Syndrom diagnostiziert. Seine Symptome verschwanden in sechs Monaten. Der Patient erlitt auch einen Herzinfarkt, aber die FDA sagte, dass dies nicht mit dem RSV-Impfstoff zusammenhängt.
Im zweiten Fall entwickelte eine Frau in den Sechzigern in Japan mit einer Vorgeschichte von Typ-2-Diabetes eine Variante des Syndroms, das sogenannte Miller-Fisher-Syndrom. Miller-Fisher betrifft tendenziell zuerst den Oberkörper, während Guillain-Barre typischerweise den Unterkörper betrifft und sich dann nach oben ausbreitet. Neun Tage nach der Impfung litt sie unter Müdigkeit und am zehnten Tag unter Halsschmerzen und schlechter Muskelkontrolle. Sie wurde 19 Tage nach der Impfung ins Krankenhaus eingeliefert. Ihre Symptome verschwanden innerhalb von drei Monaten.
Von der FDA veröffentlichte offizielle Dokumente lauten: „Angesichts des zeitlichen Zusammenhangs und der biologischen Plausibilität stimmt die FDA der Einschätzung der Prüfärzte zu, dass diese Ereignisse möglicherweise mit dem Studienimpfstoff in Zusammenhang standen. Daher wird [Guillain-Barre] als wichtiges potenzielles Risiko angesehen.“
Guillain-Barre ist eine seltene neurologische Erkrankung, bei der das Immunsystem fehlschlägt und beginnt, die Nerven des Körpers anzugreifen. In schweren Fällen kann dies zu Lähmungen, Atembeschwerden, Blutgerinnseln und Todesfällen führen. Es kann auch dazu führen, dass Patienten Schmerzen erleiden.
Es tritt normalerweise innerhalb von Tagen oder Wochen nach einer Infektion der Atemwege oder des Verdauungstrakts auf. Frühere Forschungen haben sowohl Covid- als auch RSV-Infektionen mit dem Syndrom und früheren Impfstoffen in Verbindung gebracht.
Es gibt keine Heilung für das Syndrom, aber Behandlungen sind verfügbar, die die Genesung beschleunigen können. Schätzungen zufolge haben etwa ein bis zwei Amerikaner pro 100.000 Menschen das Guillain-Barré-Syndrom. Bei den über 60-Jährigen steigt dieser Wert auf bis zu einen von 33.000 Personen.
Die Dokumente wurden vor einem Treffen zur Genehmigung des Impfstoffs nächste Woche veröffentlicht, das vom Beratenden Ausschuss für Impfstoffe und verwandte biologische Produkte (Vaccines and Related Biological Products Advisory Committee, VRBPAC) durchgeführt wird, das die Sicherheit und Wirksamkeit von Impfstoffen überprüft.
Pfizer hat zugestimmt, die Sicherheitsüberprüfung seiner klinischen Phase-3-Studie durchzuführen, der letzten Phase vor der Zulassung. In einem Briefing-Dokument schlug das Unternehmen jedoch vor, dass es möglicherweise andere Erklärungen für die Reaktionen gegeben habe. Sie fügen hinzu, dass die Impfung ein „gut verträglicher und sicherer Impfstoff mit einem günstigen Nutzen-Risiko-Verhältnis“ sei.
Derzeit ist kein Impfstoff gegen RSV verfügbar, der diesen Winter ohne Covid-Einschränkungen stark angestiegen ist. RSV ist eine häufige Infektion, die Erkältungssymptome verursacht, die innerhalb weniger Tage verschwinden. Aber es ist gefährlicher bei älteren Erwachsenen, die schwächere Immunsymptome haben und in schweren Fällen zu einer Lungenentzündung und sogar zum Tod führen können.
Die klinischen Phase-3-Studien zeigten, dass die Impfung von Pfizer zu 66,7 Prozent wirksam war, um mittelschweren Erkrankungen der unteren Atemwege mit zwei oder mehr Symptomen vorzubeugen. Es war auch zu 85 Prozent wirksam bei der Vorbeugung schwerer Krankheiten.
Dies ähnelte der von dem Pharma-Unternehmen GlaxoSmithKline entwickelten Spritze, die zu 94,1 Prozent gegen schwere Erkrankungen der unteren Atemwege und zu 82,6 Prozent bei der Vorbeugung von Krankheiten insgesamt wirksam war. In dieser Studie wurden auch Fälle von potenziellem Guillain-Barré-Syndrom erfasst, aber es gab keine ausreichenden Beweise, um eine Diagnose zu bestätigen. Daten von beiden Impfstoffen wurden am Donnerstag während einer Sitzung des Beratenden Ausschusses für Immunisierungspraktiken der Zentren für Krankheitskontrolle und Vorbeugung (Centers for Disease Control and Prevention, CDC) diskutiert.
Sie kamen zu dem Schluss, dass die Impfstoffe „bei älteren Erwachsenen eine signifikante Wirksamkeit gegen durch RSV verursachte Erkrankungen der unteren Atemwege zeigten“. Sie fügten jedoch hinzu, dass „die Überwachung nach der Zulassung sowohl für die Sicherheit als auch für die Wirksamkeit des Impfstoffs von entscheidender Bedeutung sein wird“, falls die Impfungen von der FDA genehmigt werden.
Was ist das Guillain-Barré-Syndrom?
Das Guillain-Barré-Syndrom ist eine seltene Erkrankung, bei der das Immunsystem auf Hochtouren läuft und der Körper seine eigenen Nerven angreift. Häufige Symptome der seltenen Erkrankung sind Schwäche und Kribbeln in den Gliedmaßen. Wenn sich der Zustand der Patienten verschlechtert, kann dies dazu führen, dass Teile des Körpers – oder in einigen Fällen der ganze Körper – gelähmt werden. Das Syndrom ist selten und betrifft jährlich etwa einen von 100.000 in Großbritannien und den USA.
Laut dem Nationalen Institut für neurologische Störungen und Schlaganfälle werden in den USA weniger als 20.000 Fälle pro Jahr diagnostiziert. Ärzte sagen, dass es oft durch eine virale oder bakterielle Krankheit wie Campylobacter jejuni ausgelöst wird. Es gibt kein Heilmittel. Die Behandlung konzentriert sich auf die Wiederherstellung des Nervensystems. Es kann tödlich sein, wenn es die Atemmuskulatur betrifft.
Quelle: Daily Mail
Telegram zensiert nicht! Wenn du diese Information wichtig findest, kannst du Legitim auf Telegram kostenlos abonnieren: hier anmelden (Telegram herunterladen)